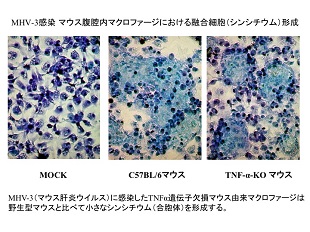
コロナウイルスの標的細胞への侵入と宿主における病原性発現機構に関する研究
メンバー: 谷口隆秀
分野: 動物生命科学、基礎医学、実験動物学
所属: 農学研究院
キーワード: ウイルス、レセプター、病態発生、マウス、発生工学
研究概要
ウイルスが感受性細胞に侵入する際には、細胞表面のウイルスレセプターとウイルスの構造タンパク質が結合することが必要であり、これらの分子の結合が鍵と鍵穴のように選択的である事がウイルス感染の「宿主特異性」や、「組織特異性」を決定しています。
しかし、本来の宿主ではない実験動物への接種を繰り返すと、本来の宿主とは異なる動物種でも感染・増殖をするようになることがあります。また、ウイルス分離時には極めて限定的な野外分離ウイルス株の培養細胞での増殖能が、継代が進むにつれて徐々に高くなり、激しく増殖するように変化する事も知られています。
本研究室ではコロナウイルスを対象として、このような現象がウイルスのどのような変化によって引き起こされるのかを解明すると共に、小型実験動物に適応したウイルス株を用いて様々な生命現象の研究を行なっています。
研究テーマ
[1]I型猫伝染性腹膜炎ウイルス (FIPV)および豚血球凝集性脳脊髄炎ウイルス(PHEV)の標的細胞への侵入機構の解明と感染標的細胞における病態形成機構について
I型FIPVおよびPHEVがどのようなウイルス受容体を用いてどのように標的細胞へ感染するのか、またマクロファージや神経細胞のような標的細胞におけるウイルスの動態・病原性発揮の機構について研究を進めています。
[2]PHEVを用いたニューロトレーシング
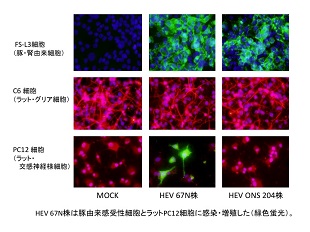
豚血球凝集性脳脊髄炎ウイルス(PHEV)67N株が齧歯類の神経細胞に感染し、シナプスを経由して接続している神経細胞に感染が拡がる性質を利用して、神経接続の追跡(ニューロトレーシング)に適したHEVの開発を目指しています。
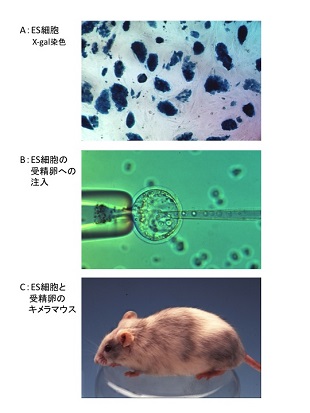
[3]遺伝子改変技術を用いた実験動物の作出と利用
免疫関連遺伝子の欠損マウスを用い、ウイルス感染がどのような機構で病態を形成するのか明らかにするとともに、猫や豚などを宿主とするウイルスのレセプターを発現する家畜ウイルス感染モデルマウスの作出を目指しています。
主要論文・参考事項
1.Neurotropic Virus Tracing Suggests a Membranous-Coating Mediated Mechanism for Transsynaptic Communication. Yan-Chao Li, Wan-Zhu Bai, Norio Hirano, Tsuyako Hayashida, Takahide Taniguchi, Yoichi Sugita, Koujiro Tohyama, Tsutomu Hashikawa. J. Comp. Neurol. (2013) 521:203-212.
2. Tumor necrosis factor alpha is not a pathogenic determinant in acute lethal encephalitis induced by a highly neurovirulent strain of mouse hepatitis virus. Kazuya Shirato, Eiichi Momotani, Masuhiro Takata, Kenji Sekikawa, Takahide Taniguchi. Arch Virol. (2008) 153:549–553.
3. Susceptibility of heat shock protein 70.1-deficient C57BL/6 J, wild-type C57BL/6 J and A/J mice to Trypanosoma congolense infection. Yoshio Nakamura, Jan Naessens, Masuhiro Takata, Takahide Taniguchi, Kenji Sekikawa, John Gibson, Fuad Iraqi. Parasitol. Res. (2003) 90:171–174.
4. HSP70 Protects against TNF-Induced Lethal Inflammatory Shock. Wim Van Molle, Ben Wielockx, Tina Mahieu, Masuhiro Takada, Takahide Taniguchi, Kenji Sekikawa, Claude Libert. Immunity. (2002) 16:685–695.
5. Failure of germinal center formation and impairment of response to endotoxin in tumor necrosis factor alpha-deficient mice. Takahide Taniguchi, Masuhiro Takata, Akemi Ikeda, Eiichi Momotani, Kenji Sekikawa. Lab. Invest. (1997) 77:647-658.
お問い合わせ先
東京農工大学・先端産学連携研究推進センター
urac[at]ml.tuat.ac.jp([at]を@に変換してください)
Studies on the mechanisms of coronavirus invasion to target cells and pathogenesis on host animals.

Research members: Dr. Takahide Taniguchi
Research fields: Animal life science, Basic medicine, Laboratory animal science
Departments: Institute of Agriculture
Keywords: virus, receptor, pathogenic mechanism, mouse, developmental engineering
Summary

In the event of viral infection, it is very important that viral structural protein interact with specific virus receptor on susceptible cell surface. Selective interaction of virus-virus receptor decide “host specificity” and “tissue specificity”.
However, when viruses inoculated to non-natural host animal iteratively, some viruses change their host specificity and propagated in non-natural host. Viruses get acclimatized to non-natural host and propagate in that animal.
When viruses isolate from field samples using cultured cells in vitro, at first field isolated virus strain propagate very little. However, continuously-cultivated field isolate have come to proliferate in cell culture.
In our laboratory, we are researching about invasion mechanisms to target cells and this adaptation phenomenon by targeting coronaviruses. We are also researching about various phenomena induced by coronavirus infection in target cells (neuronal cell, macrophage etc.).
Major research themes
[1]Studies on the invasion mechanism and pathogenesis of feline infectious peritonitis virus
(FIPV) type I and porcine hemagglutinating encephalomyelitis virus (PHEV) in target cells.
[2]Development of safety neurotracing tool using PHEV
PHEV 67N strain infect to rodent’s nerve cells and the virus infection spread
transsynaptically. We are researching this coronavirus strain to develop a new
neurotracing tool.
[3]Production and utilization of genetically engineered mouse
We are researching pathogenic mechanisms on coronavirus infection using immunity-related
gene KO mouse. In addition, we aim to develop domestic animal virus infection model mouse
that express domestic animal virus receptor.
Reference articles and patents
1.Neurotropic Virus Tracing Suggests a Membranous-Coating Mediated Mechanism for Transsynaptic Communication. Yan-Chao Li, Wan-Zhu Bai, Norio Hirano, Tsuyako Hayashida, Takahide Taniguchi, Yoichi Sugita, Koujiro Tohyama, Tsutomu Hashikawa. J. Comp. Neurol. (2013) 521:203-212.
2. Tumor necrosis factor alpha is not a pathogenic determinant in acute lethal encephalitis induced by a highly neurovirulent strain of mouse hepatitis virus. Kazuya Shirato, Eiichi Momotani, Masuhiro Takata, Kenji Sekikawa, Takahide Taniguchi. Arch Virol. (2008) 153:549–553.
3. Susceptibility of heat shock protein 70.1-deficient C57BL/6 J, wild-type C57BL/6 J and A/J mice to Trypanosoma congolense infection. Yoshio Nakamura, Jan Naessens, Masuhiro Takata, Takahide Taniguchi, Kenji Sekikawa, John Gibson, Fuad Iraqi. Parasitol. Res. (2003) 90:171–174.
4. HSP70 Protects against TNF-Induced Lethal Inflammatory Shock. Wim Van Molle, Ben Wielockx, Tina Mahieu, Masuhiro Takada, Takahide Taniguchi, Kenji Sekikawa, Claude Libert. Immunity. (2002) 16:685–695.
5. Failure of germinal center formation and impairment of response to endotoxin in tumor necrosis factor alpha-deficient mice. Takahide Taniguchi, Masuhiro Takata, Akemi Ikeda, Eiichi Momotani, Kenji Sekikawa. Lab. Invest. (1997) 77:647-658.
Contact
University Research Administration Center(URAC),
Tokyo University of Agriculture andTechnology
urac[at]ml.tuat.ac.jp
(Please replace [at] with @.)